
肿瘤的发展除了与癌细胞自身基因突变导致的恶性增殖有关以外,还与肿瘤微环境息息相关。在癌症中,正常组织中和谐的细胞相互作用关系被破坏,原本保护正常细胞生存的微环境在肿瘤细胞的影响下,逐渐演变成适应肿瘤生长的条件。针对肿瘤微环境的检测和表征研究也可为癌症治疗提供新的思路。
目前空间多组学技术已用于研究几种类型癌症中肿瘤免疫微环境的转录组、蛋白质组和代谢组,从这些方法获得的数据已与免疫组化和多参数分析相结合,以产生癌症进展的标记物。传统分析技术受样品空间分辨率以及分析灵敏度的限制,无法精准获取靶向部位,而对其中特异代谢物的差异表征就更加困难。组织切片伴随着显微镜技术等的发展而得到广泛的应用,而激光显微切割 (LMD, laser microdissection) 技术(如使用Leica LMD6/7)可以方便地对特定的组织区域进行精确分离(图2)。结合高灵敏度的液质联用检测技术,基于SCIEX的ZenoTOF® 7600 系统,将空间定位准确的微区细胞代谢谱进行全面准确的表征。代谢谱是免疫微环境的重要调节因子,可能通过影响癌细胞的增殖潜能和适应环境而发挥作用。代谢特征的异质性似乎有助于肿瘤免疫微环境的异质性。

图1. 激光显微切割-空间多组学质谱分析流程
肿瘤微区样品制备
由制备好的肿瘤组织切片样本置于激光显微切割载物台,确定好焦距平面后,将视野移动到待切割的细胞区域(先通过H&E染色的平行样本确定肿瘤组织分区),在调节好相关参数后开始进行切割。通过对样本分别进行水溶性代谢物和脂溶性代谢物的提取,进而进行基于液质联用系统的全面的代谢组学分析。
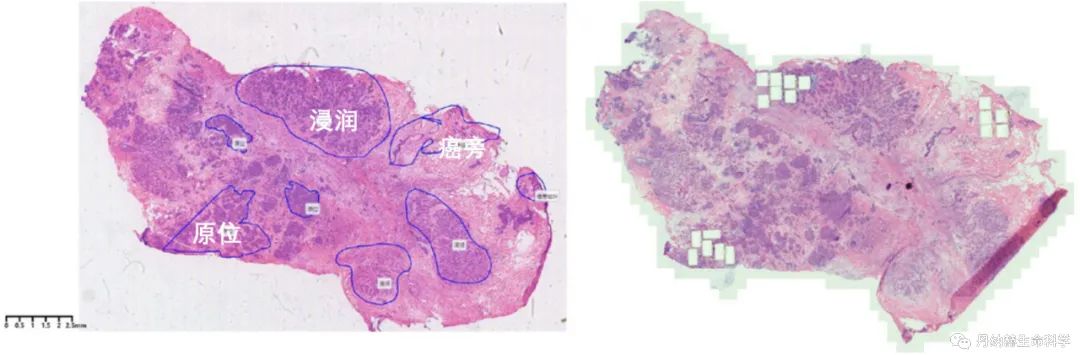
图2. 组织切片样本用于激光显微切割分离体制备。经过苏木精-伊红(HE)染色确定组织切片中不同类型的细胞区域(左)包括原位癌、浸润癌和癌旁细胞,在平行的未染色组织切片中的相应位置进行激光显微切割获得分离体(右)。
Leica 激光显微切割系列产品利用UV激光可直接从组织切片制备分子生物分析所需的样品,可用于基因组学、转录物组学、蛋白质组学、代谢物组学和活细胞应用等的快速、精确且高质量的切割。
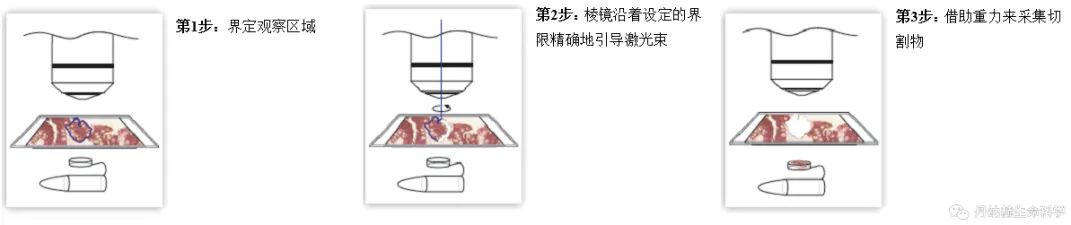
图3. 徕卡激光显微切割流程(通过重力作用收集感兴趣区域)
代谢物全面表征 组织细胞中代谢物成分复杂多样,且有较多同分异构体,仅有准确的高分辨一级无法对化合物进行确证。针对大量样本,SCIEX OS软件可自动进行峰提取和搜库,通过一级质量数、同位素丰度和二级碎片的匹配对样本中的代谢物进行鉴别(图3),使筛查流程快速准确。在代谢组学的样本中共鉴定173个化合物,包括氨基酸类、核苷类、吲哚类、脂肪酸类等。
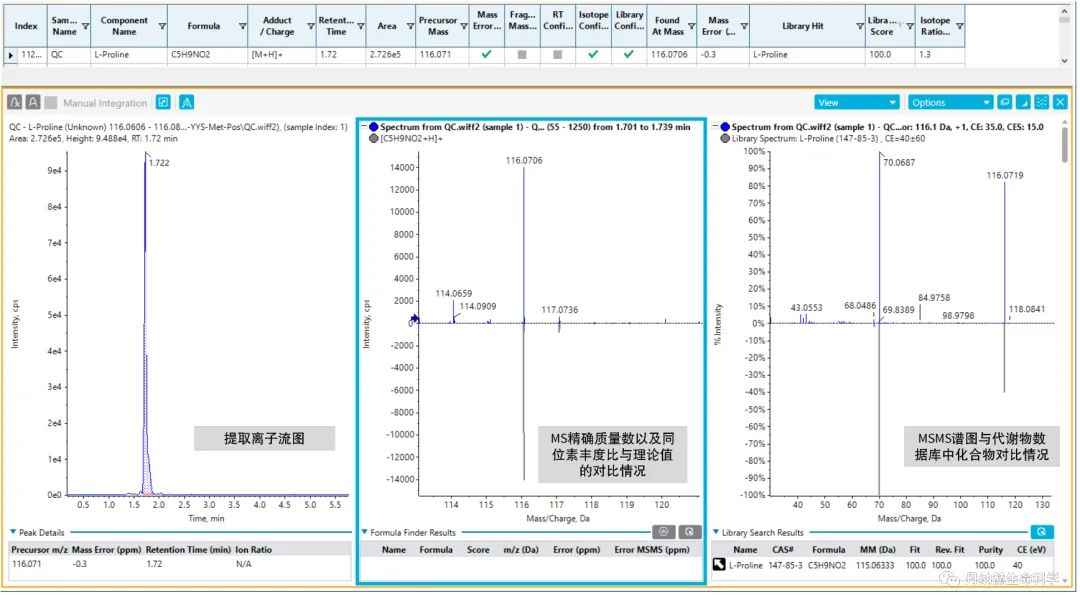
图4. 代谢物鉴定界面示例。以样本中鉴定到的脯氨酸(Proline)为例,Proline分子式为C5H9NO2,检测到的MS信号与理论质荷比相比,质量数偏差为-0.3ppm,同位素丰度比与理论值偏差为1.3%,MSMS与代谢物库中Proline的标准谱图匹配度为100,以此可判定鉴定到的信号为Proline。
在脂质组学分析样本中共鉴定到550个脂质化合物,基于ZenoTOF® 7600 系统特有的电子活化解离(EAD)碎裂模式,可以鉴定出其中一些脂质化合物的精细结构,如脂肪酸链连接的具体位置(sn1或sn2)以及连接的不饱和脂肪酸双键的具体位置(图4);对于样本中检测到的脂质化合物包括固醇酯类、神经酰胺类、溶血磷脂胆碱类、磷脂胆碱类、溶血磷脂乙醇胺类、磷脂乙醇胺类、磷脂肌醇类、磷脂丝氨酸类、鞘酯类、甘油二酯类、甘油三酯类。
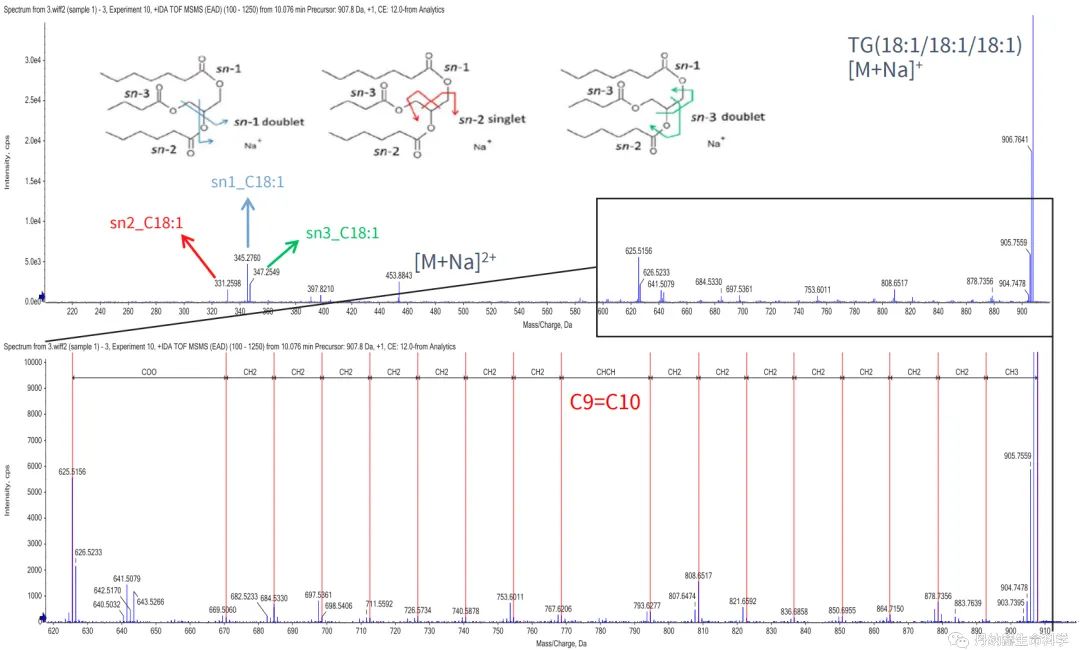
图5. 脂质化合物精细结构鉴定示例。以甘油三酯TG (18:1/18:1/18:1)为例,在EAD碎裂模式下,化合物[M+Na]+峰可以产生特征的碎片离子,帮助解析甘油三个羟基各自所连接的脂肪酸组成,以及在高质荷比区域产生的连续CH2断裂碎片确定不饱和键的位置(C9和C10间为双键)。
差异代谢物分析 在质控样本(quality control, QC, 所有样本等体积混合,整个分析批次中每6个样本穿插一针QC样本进样)中,化合物峰面积RSD%不超过30%(n=8),在代谢组学样本中共检出100个代谢物,脂质组学样本中共检出502个代谢物,并将这些化合物在所有的样本包括原位癌组织、浸润癌组织、癌旁组织进行峰面积提取。
将获得的各种组织中化合物含量信息进行生物统计学分析,以浸润癌组织v.s.癌旁组织为例,共找到84个差异代谢物(图5)。经过后续进一步生物学验证,确定的差异代谢物可以帮助开展癌细胞在空间定位及异质性的精准区分工作,更好的理解例如肿瘤转移的起源和发展、侵袭能力、对药物的敏感性等方面的特点,从而制定个体化的精准治疗方案。
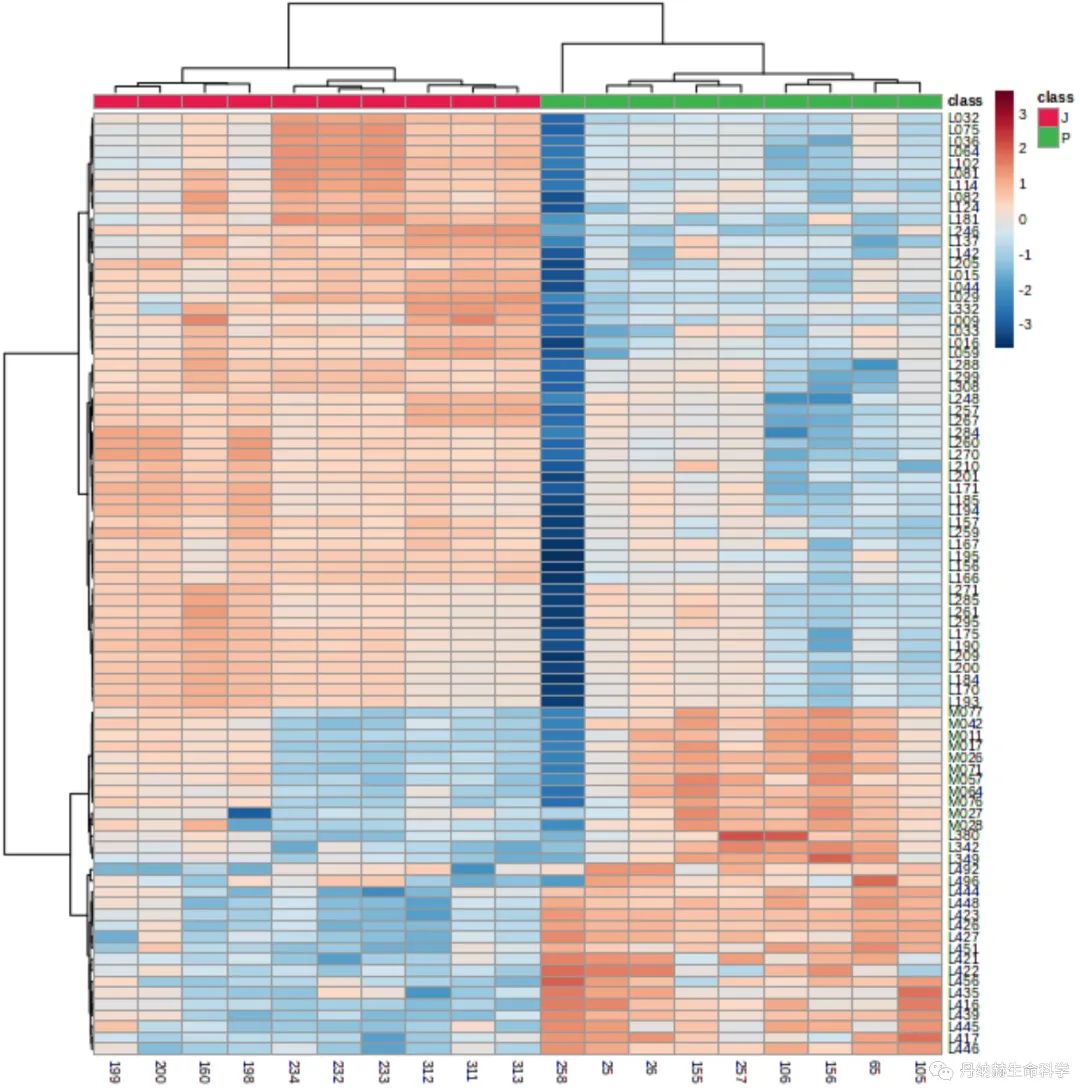
图6. 浸润癌组织v.s.癌旁组织中的差异代谢物热图。通过统计学分析,包括t-test的p值小于0.05以及PLSDA计算的VIP值不小于1作为筛选条件,获得了84个差异代谢物。
总结 通过对组织切片进行激光显微切割获取空间定位准确的微量样本,并与SCIEX ZenoTOF® 7600 系统相结合,实现微量细胞水溶性和脂溶性代谢物的全面表征以及高灵敏度组学分析。可将此方案应用于其他组织切片样本,助力空间多组学研究的开展。
感谢厦门大学生命科学学院林树海教授及其课题组成员华铮翼、姚博对方案中组织切片和样本制备的支持;
感谢丹纳赫生命科学平台徕卡显微系统公司高天龙、连其林对显微切割技术的支持。
空间多组学研究LMD平台:
徕卡激光显微切割系统
Leica LMD7
激光显微切割(LMD)是一种适用于精确制备样品的技术。在许多研究领域,它是获得纯净的、单一的后续实验起始材料的先决条件。在基因组学、转录组学、微阵列、二代测序、生物芯片和蛋白质组学等领域中,需要使用这项高精度技术以进行有意义的分析。Leica LMD系列用UV激光直接从组织切片制备分子生物分析所需的样品。随着创新方法和仪器的不断开发,激光显微切割在其他领域的应用也日益广泛,如活细胞研究、气候研究和电子显微镜的玻片雕刻。现在,研究人员正在以前所未有的水平使用LMD来最大化影响他们的研究。
徕卡显微系统为用户提供了一种精确、高度选择性的激光显微切割方法,可用于如下各种应用:
► 快速、精确地分离超纯细胞和细胞群;
► 用于基因组学、转录物组学、蛋白质组学、代谢物组学和活细胞应用的高质量切割;
► 方便地使用激光制备活细胞和其他样品;
► 标记和可追溯显微镜下的样品。
空间多组学研究质谱平台: 多重碎裂高分辨质谱 SCIEX ZenoTOF® 7600 系统
ZenoTOF® 7600 系统于2021年推出即获得国际“分析科学家创新奖”之首,集成了多项前沿新技术,包括: ► 能实现更高二级质谱灵敏度的Zeno™ Trap (Zeno 阱) 技术; ► 能与经典CID碎裂技术互补的电子活化解离 (EAD) 技术; ► 升级的133Hz超快速二级质谱扫描能力; ► 新一代全景质谱Zeno SWATH® DIA数据依赖型采集技术等。
多重碎裂质谱ZenoTOF® 7600 系统的卓越性能,大大提升生命科学多组学研究的深度和广度,尤其在高通量高深度蛋白质组学、蛋白质翻译后修饰(尤其是糖蛋白质组学)、全景非靶向代谢组学、脂质精细结构解析等尖端领域获得广泛应用。

